文章最后更新时间:2024-08-12 19:17:57,由春晓健康网负责审核发布,若内容或图片失效,请留言反馈!
首款中国原研合源生物CD19 CAR-T产品纳基奥仑赛(源瑞达、CNCT19细胞注射液)获批上市
纳基奥仑赛获批上市
2023年11月8日,我们又迎来一个重磅好消息!根据中国国家药监局(NMPA)官网显示,合源生物自主研发的CAR-T产品源瑞达®(纳基奥仑赛注射液,Inaticabtagene Autoleucel Injection,CNCT19细胞注射液)的新药上市申请(NDA)已获得正式批准,用于治疗成人复发或难治性B细胞急性淋巴细胞白血病(r/r B-ALL)。
据无癌家园小编得知,纳基奥仑赛注射液是首款具有中国全自主知识产权CD19 CAR-T细胞治疗产品,也是首款在中国获批上市的治疗白血病的CAR-T产品!

截图源自NMPA官网
纳基奥仑赛注射液是通过基因修饰技术将靶向 CD19 的嵌合抗原受体(CAR)表达于 T 细胞表面而制备成的自体 T 细胞免疫治疗产品。输注至体内后会与表达 CD19 的靶细胞结合,激活下游信号通路,诱导 CAR-T 细胞的活化和增殖并产生对靶细胞的杀伤作用。
此前,纳基奥仑赛注射液就已获得国家药品监督管理局授予的“突破性治疗药物”认定,其获批上市将在疗效、安全性及治疗便捷性上给成人r/r B-ALL患者带来突破性的临床治疗选择。
持久缓解且伴长期生存获益,纳基奥仑赛剑指白血病
纳基奥仑赛注射液是首款在中国获批上市的治疗白血病的CAR-T产品,也是第四款上市的CAR-T疗法。其临床研究数据早在2022年12月的第64届美国血液学会(ASH)年会上进行过口头报告。截止到2022年9月27日,39例成人r/r B-ALL患者接受了纳基仑赛注射液回输,细胞产品制备成功率100%,其结果显示:
●3个月内的总体缓解率(ORR)高:在39例患者中,有32例患者达到不同程度的缓解,3个月内的ORR为82.1%!
●3个月时的总体缓解率(ORR)高:在39例患者中,经IRC评估有25例患者达到不同程度缓解,3个月时的ORR为64.1%。
●CR(完全缓解)率高:32例3个月内获得ORR的患者中,26例为CR,CR率达66.7%(26/39)。25例3个月时获得ORR的患者中,20例为CR,CR率达51.3%(20/39)。
●MRD阴性率高:3个月时和3个月内达CR或CRi患者中MRD阴性率分别为92.0%和100%。
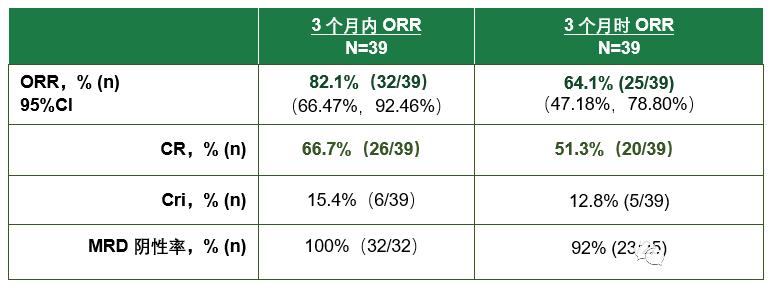
有效性数据总结
上述结果表明,接受纳基奥仑赛注射液治疗后,达到缓解的患者,显示出持久的缓解、长期的无复发生存期及总生存期。在3个月时仍处于缓解的患者中,预计有80%患者在1年时仍持续缓解;且患者无论后续是否接受造血干细胞移植,均能表现出持续缓解和长期生存获益。
临床试验招募
目前急招B细胞淋巴瘤、T细胞淋巴瘤、T细胞白血病(T-ALL)、急性淋巴细胞白血病、非霍奇金淋巴瘤、胃癌、肝癌、胰腺癌、结直肠癌、间皮瘤、卵巢癌等癌种!
想要评估病情是否能够接受CAR-T疗法可将病理报告、治疗经历及出院小结等提交至无癌家园医学部进行初步评估







发表评论