文章最后更新时间:2024-08-12 20:16:45,由春晓健康网负责审核发布,若内容或图片失效,请留言反馈!
瑞士制药巨头罗氏(Roche)近日在德国慕尼黑举行的2018年ESMO上公布了PD-L1肿瘤免疫疗法Tecentriq(atezolizumab)联合Avastin(bevacizumab,贝伐单抗)治疗不可切除性或晚期肝细胞癌(HCC)的Ib期临床研究(NCT02715531)的数据。
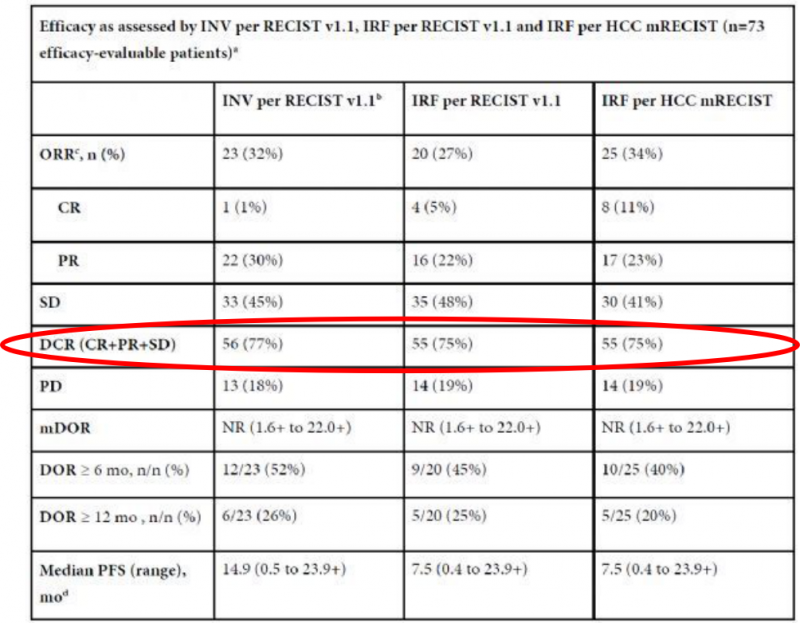
疗效评估群体包括所有接受联合治疗并被随访至少16周的患者,中位生存随访时间为7个月。完全缓解率(CR)方面,INV根据RECIST v1.1评估的CR为1例(1%),IRF根据RECIST v1.1评估的CR为4例(5%),IRF根据HCC mRECIST评估的CR为8例(11%)。疾病控制率(DCR,即经历缓解或稳定病情)在所有形式的评估中都保持一致,INV根据RECIST v1.1评估的DCR为77%(n=56/73),IRF根据RECIST v1.1评估以及根据HCC mRECIST评估的DCR均为75%(55/73)。中位缓解持续时间(DOR)和总生存期(OS)还没有达到。
在安全性可评估群体(n=103)中,27%的患者(n=28/103)经历3-4级治疗相关不良事件,2%(n=2/103)经历治疗相关的5级不良事件。除了现有单个药物的安全概况之外,没有发现与联合治疗相关的新的安全信号。
今年7月,美国FDA根据正在进行的Ib期研究的总体数据,已授予Tecentriq+Avastin组合疗法一线治疗晚期或转移性肝细胞癌的突破性药物资格(BTD)。这也是罗氏产品组合中迄今为止被授予的第23个BTD,也是Tecentriq迄今被授予的第3个BTD。
http://news.bioon.com/article/6728996.html
声明:春晓健康网是服务与广大癌症肿瘤客户群体的综合性网站,提供癌症肿瘤相关问题交流咨询等服务,有这方面的需要可以直接点击右侧在线客服进行交流以及咨询!







发表评论