 淋巴瘤
淋巴瘤淋巴瘤FDA:淋巴瘤一线治疗后耐药有新药啦!
2018年6月8日,美国FDA批准venetoclax(VENCLEXTA,AbbVie Inc.和Genentech Inc.)用于慢性淋巴细胞白血病(CLL)或小淋巴细胞性淋巴瘤(SLL)患者,伴或不伴17p缺失,患者至少接受了一次治疗。 批准是基于MURANO(NCT02005471),一项随机(1:1)、多中心、开放标签的试验,对比利妥昔单抗联合v
 淋巴瘤
淋巴瘤2018年6月8日,美国FDA批准venetoclax(VENCLEXTA,AbbVie Inc.和Genentech Inc.)用于慢性淋巴细胞白血病(CLL)或小淋巴细胞性淋巴瘤(SLL)患者,伴或不伴17p缺失,患者至少接受了一次治疗。 批准是基于MURANO(NCT02005471),一项随机(1:1)、多中心、开放标签的试验,对比利妥昔单抗联合v
 淋巴瘤
淋巴瘤肥胖不仅有悖于国人的审美,还会导致诸多慢性病。在一些研究中表明体重指数(BMI)与某些部位(如消化系统)癌症发病风险呈相关,但与其他部位癌症的关系尚无统一结论。2017年底发表在Annals of Oncology的一项umbrella review,综合分析了26项BMI与癌症发病风险之间关系的meta分析,力求为读者带来最的结论。 研究只纳入评价BMI
 淋巴瘤
淋巴瘤在2018年初,桑德拉林伯格在CAR T细胞疗法被批准后的几个月接受了治疗。仅仅一个月,她的淋巴瘤就完全消失了 - 医生说,她已经完全缓解了。 “那些小小的免疫细胞一直在控制它,”Linberg说,她一直没有复发。 75岁的Linberg来自马萨诸塞州费尔黑文市,很幸运,她在最危急的时候选择了CAR T治疗。她之前接受过晚期非霍奇金淋巴瘤的标准化疗治疗,虽
 淋巴瘤
淋巴瘤CART治疗淋巴瘤,淋巴瘤CAR-T临床试验招募进行中著名《新闻联播》主持人罗京、在《情深深雨濛濛》里扮演方瑜的演员李钰、以《滚蛋吧!肿瘤君》感动了众多网友的漫画家熊顿……这些年,不少名人都因为淋巴瘤离开了人世。淋巴瘤成夺命杀手,称"最会伪装的疾病"据统计,全世界每9分钟就有1个淋巴瘤新发病例。我国淋巴瘤发病率为0.02‰,每年新增病人约2.5万人,死亡人数
 白血病
白血病FDA已经更新了尼罗替尼nilotinib (Tasigna,诺华)用药停止的标签说明。 2007年,Nilotinib获得了FDA的批准,用于治疗费城染色体阳性(Ph+)慢性骨髓白血病(CML)的患者。 指南建议,大多数通过酪氨酸激酶抑制剂治疗获得缓解的患者会继续服用药物,但目前还不清楚是否持续用药对所有患者都是必要的。 更新后的剂量推荐表明,长期使用尼罗
 淋巴瘤
淋巴瘤来自Wellcome Sanger研究所科学家们发现,可能在确诊之前几年就能发现患有急性髓性白血病(AML)的高风险人群,患有AML的患者在突然发病之前血液中已经存在遗传变化。 研究发表在“自然”杂志上,通过寻找DNA突变的血液检测可以揭示健康人群中AML的根源。进一步的研究可以在未来更早发现和监测有AML风险的人,并开辟阻止患癌的方法。 急性髓性白血病
 淋巴瘤
淋巴瘤Eagle Pharmaceuticals宣布其稀释即用的(ready-to-dilute,RTD)盐酸苯达莫司汀(bendamustine hydrochloride)溶液获得了美国FDA的最终批准,用于治疗慢性淋巴性白血病(CLL)和惰性B细胞非霍奇金淋巴瘤(NHL)。该注射液无需重新溶解,可在30或60分钟内以500毫升混合溶液形式给药。 CLL是一种
 淋巴瘤
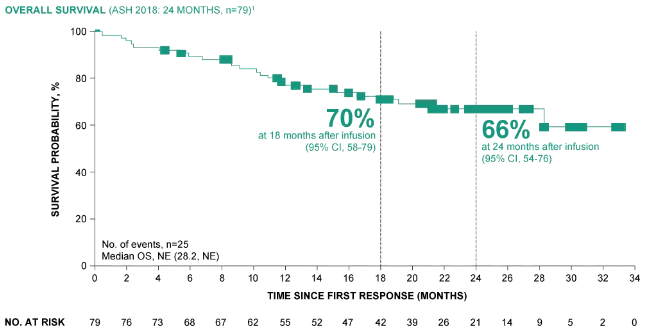
淋巴瘤根据第二阶段的研究结果,标准护理化疗药物阿扎胞苷与免疫检查点抑制剂nivolumab(纳武单抗)的组合显示,复发或难治性急性髓细胞白血病(AML)患者的反应率和总生存率令人鼓舞。 该研究随访了70名患者,经过平均2线治疗后复发性AML,报告总体反应率为33%,完全缓解率为22%。该药物组合对于之前未接受过低甲基化试剂(HMA)如阿扎胞苷或地西他滨治疗的患者
 淋巴瘤
淋巴瘤Forty Seven公司在ASCO年会上公布了新型肿瘤免疫疗法5F9的两个独立临床试验的概念验证性数据。第一项1b/2期临床试验在复发性/难治性非霍奇金淋巴瘤患者(r/r NHL)中,评估了5F9联合利妥昔单抗(rituximab)的疗效。第二项1期临床试验在晚期实体瘤患者中,评估了5F9的药代动力学(PK)和药效学(PD)。 Forty Seven的5
 淋巴瘤
淋巴瘤1、基因表达模型预测滤泡性淋巴瘤的无进展生存期!基于“稳健”23基因表达模型成功预测了III期随机PRIMA试验中纳入的滤泡性淋巴瘤患者的无进展生存期(PFS)。 研究人员确定了395个与进展风险相关的基因,其中23个纳入了基于B细胞生物学和肿瘤微环境的预测模型。在根据利妥昔单抗(Rituxan)维持治疗和滤泡性淋巴瘤国际预后指数1(FLIPI-1)得分调整
 淋巴瘤
淋巴瘤FDA接受克唑替尼成为儿童淋巴瘤靶向药物新药申请,整体缓解率可达90%2020年9月24日,辉瑞公司发布公告称,FDA接受了辉瑞公司提交的克唑替尼补充新药申请,用于治疗ALK阳性的间变性大细胞淋巴瘤小儿患者的新适应症。FDA将于2021年1月前就此申请做出批复。A8081013研究:完全缓解率44%,整体缓解率50%该研究共纳入44例患儿,其中18例为淋巴瘤
 淋巴瘤
淋巴瘤美国FDA刚刚批准gilteritinib(Xospata)用于治疗FLT3突变阳性复发或难治性急性髓性白血病(AML)的成年患者。 与gilteritinib一起使用时,还授予伴随诊断基因检测技术。由Invivoscribe Technologies,Inc开发的LeukoStrat CDx FLT3突变检测法用于检测AML患者的FLT3突变。 “大约2
 白血病
白血病速递|慢性粒细胞白血病新药Asciminib(Scemblix)获FDA加速批准2021年10月30日,FDA加速批准了Asciminib(Scemblix)的新适应症申请,用于治疗Ph阳性的慢性粒细胞白血病慢性期患者。这些患者应当已经接受过至少2种靶向方案治疗。除此以外,FDA还同时将Asciminib治疗T315I突变的Ph阳性慢性粒细胞白血病慢性期患者
 淋巴瘤
淋巴瘤昨日,我们刚刚报道了FDA对于K药用于治疗宫颈癌的批准,今日再添喜讯,K药又一适应症获批。就在昨天,美国FDA批准pembrolizumab(Keytruda,派姆单抗)用于治疗难治性原发性纵隔大B细胞淋巴瘤(PMBCL)的成人和儿科患者,曾至少使用两线治疗后仍旧复发。 批准是基于来自多中心,开放标签,单臂试验KEYNOTE-170(NCT02576990
 白血病
白血病嘌呤类似物治疗毛细胞白血病(HCL)疗效显著,但高达50%患者治疗后复发。Tiacci等人2011年研究发现HCL的遗传学病因为BRAF V600E突变。2015年,Tiacci与Park等人研究发现,对HCL患者给予中位给药16周BRAF抑制剂vemurafenib(威罗菲尼)治疗,高达96%的患者对治疗产生应答。中位给药8周后,即可产生应答,其中35%的
 白血病
白血病CAR-T治疗急性白血病为患者带来曙光Kymriah:治疗急性淋巴细胞白血病,MRD阴性率高达80%Kymriah是一种针对CD19的CAR-T免疫细胞疗法,除了获批治疗复发或难治性弥漫大B细胞淋巴瘤外,还可用于治疗儿童和年轻人(≤25岁)B细胞急性淋巴细胞白血病(ALL)。一项关于“Kymriah治疗B细胞ALL的Ⅱ期临床试验(NCT02228096)”,
 淋巴瘤
淋巴瘤淋巴是分布在人体的全身部位的,错综复杂,一般看淋巴人们首先想到的就是脖子,其实腋下和腹股沟都存在的,淋巴结的出现也不要认为一定就是癌症,其实要是及早的控制住还是没有危险的,人们对淋巴癌的了解不多,所以存在着很多的错误认知,早点认清楚,也不至于耽误治疗。淋巴癌的误区都有哪些呢?1、颈下淋巴肿大就是淋巴瘤当身体某个部位出现炎症时,可能会引起淋巴结的肿大,比
 淋巴瘤
淋巴瘤DNA甲基化是AML中最常见的表观遗传学改变及重要的发病机制之一,并且DNA甲基化状态与AML的预后具有密切相关性。多年以来中国市场获批的去甲基化药物寥寥无几。近来,维达莎(阿扎胞苷)终于被CFDA批准用于AML的治疗。2018年3月17日的百济神州血液论坛上将宣布这一重要上市信息。但值得指出的是:DNA甲基化是可逆性改变。因此,这也为AML的治疗提供了明确
 淋巴瘤
淋巴瘤一项多中心III期临床试验的结果显示,老年慢性淋巴细胞白血病(CLL)患者如果使用新的靶向药物依鲁替尼治疗对比之前常用有效的方案——苯达莫司汀联合利妥昔单抗疾病进展率显着降低,也表明利妥昔单抗联合依鲁替尼不会带来超过单用依鲁替尼的额外益处。 CLL是老年人中最常见的白细胞癌。2016年,美国FDA批准依鲁替尼作为CLL的一线治疗药物。以前的研究表明,依鲁替
 白血病
白血病FDA授予NMT抑制剂PCLX-001治疗急性髓细胞白血病孤儿药资格急性髓细胞白血病(AML)是细胞髓系造血干细胞恶性血液疾病,占小儿白血病的30%,多数病例病情急重,预后凶险。依据现有疗法,患者复发率较高,20岁及以上的AML患者的5年生存率仅为27%。患者亟待研究人员开发出针对AML的新药!近日,美国FDA传来喜讯,授予 PCLX-001孤儿药称号(OD