文章最后更新时间:2025-03-12 17:00:02,由春晓健康网负责审核发布,若内容或图片失效,请留言反馈!
本文介绍了胃癌FGFR2b靶点靶向药试验,强调其在胃癌治疗中的重要作用。文章阐述了FGFR2b靶点与胃癌的关系,以及该靶向药试验的优势,如高度选择性、显著效果和良好安全性。同时,公布了试验招募信息,并探讨了参与试验的意义,包括提高患者生存率、推动医学发展和实现个性化治疗。全球好药网将提供最新抗癌药物信息,助力胃癌患者获得更好的治疗。
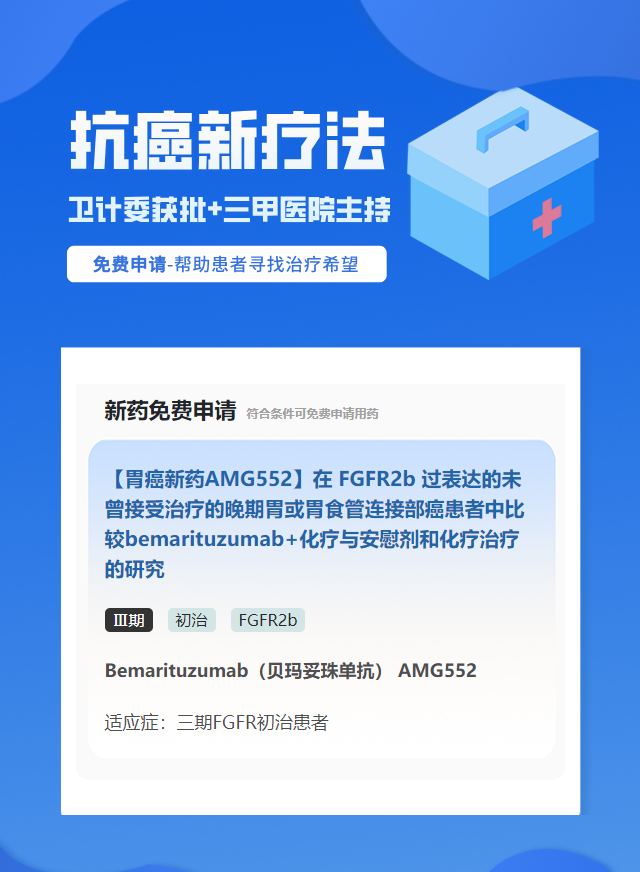
【石嘴山】胃癌FGFR2b靶点靶向药免费试验
项目名称:【胃癌新药AMG552】在 FGFR2b 过表达的未曾接受治疗的晚期胃或胃食管连接部癌患者中比较bemarituzumab+化疗与安慰剂和化疗治疗的研究
药品名称:Bemarituzumab(贝玛妥珠单抗) AMG552
基因分型:靶向药
突变基因:FGFR2b
临床期数:Ⅲ期
治疗线数:初治
适应症状:三期FGFR初治患者
项目优势:Bemarituzumab(贝玛妥珠单抗) 是全球首个(first-in-class)靶向FGFR2b的人源化单克隆抗体,主要通过两种方式发挥抗肿瘤作用:1.阻断肿瘤FGFR2b受体抑制其生长信号通路;2.增强NK细胞及巨噬细胞ADCC作用。

【石嘴山】胃癌FGFR2b靶点靶向药免费试验
一、胃癌FGFR2b靶点靶向药试验简介
胃癌是一种常见的恶性肿瘤,严重威胁着全球人类的生命健康。随着分子生物学研究的不断深入,胃癌的治疗已经从传统的化疗、放疗逐渐转向了精准治疗。胃癌FGFR2b靶点靶向药试验,正是基于这一理念,为患者提供了一种新的治疗选择。
二、FGFR2b靶点与胃癌的关系
FGFR2b是纤维生长因子受体2b(Fibroblast Growth Factor Receptor 2b)的简称,是一种在胃癌细胞中常见的基因突变。研究表明,FGFR2b基因突变与胃癌的发生、发展密切相关。针对FGFR2b靶点的靶向药物,可以有效抑制胃癌细胞的生长,为患者带来治疗希望。
三、胃癌FGFR2b靶点靶向药试验的优势
1. 高度选择性:靶向药物针对FGFR2b基因突变,具有高度选择性,避免了传统化疗药物对正常细胞的损伤。
2. 效果显著:临床试验表明,胃癌FGFR2b靶点靶向药物在抑制肿瘤生长方面具有显著效果,部分患者甚至实现了肿瘤缩小。
3. 安全性好:与传统化疗药物相比,靶向药物的不良反应相对较少,患者耐受性更好。
四、胃癌FGFR2b靶点靶向药试验招募信息
为了进一步验证胃癌FGFR2b靶点靶向药物的效果,我国多家医疗机构联合开展了一项临床试验,现正面向全国招募患者。以下是招募信息:
招募对象:经病理学检查确认为胃癌,且FGFR2b基因突变阳性的患者。
试验药物:FGFR2b靶点靶向药物。
试验地点:全国多家医疗机构。
报名方式:拨打全球好药网咨询热线:400-119-1082,或通过全球好药网官方网站报名。
五、参与胃癌FGFR2b靶点靶向药试验的意义
1. 提高患者生存率:通过参与试验,患者有机会使用到先进的靶向药物,提高生存率。
2. 推动医学发展:胃癌FGFR2b靶点靶向药试验的成功,将为我国胃癌治疗提供新的思路,推动医学发展。
3. 个性化治疗:试验结果将为患者提供更精准的个体化治疗方案,提高治疗效果。
六、温馨提示
胃癌FGFR2b靶点靶向药试验为胃癌患者带来了新的治疗希望。全球好药网作为专业的抗癌新药信息交流平台,将密切关注试验进展,为患者提供最新、最全面的抗癌药物信息。如果您或您的家人符合招募条件,欢迎拨打全球好药网咨询热线:400-119-1082,了解试验详情。让我们共同期待精准治疗为胃癌患者带来更好的生活质量。
入选标准
1.在开始任何研究特定的活动/程序前,受试者已提供知情同意。
2.年龄≥18 岁(或国内法定成人年龄,以年龄较大者为准)
3. 组织学记录的胃或胃食管连接部腺癌(不能进行根治治疗)。
• 原发肿瘤部位将按照美国癌症联合委员会 / 国际癌症控制联盟[AJCC/UICC]第 8 版进行分类。
4.不可切除的、局部晚期或转移性疾病(不能进行根治治疗)
5.基于存档(在签署预筛选知情同意书前 6 个月/180 天内获得)或新鲜活检肿瘤样本,通过在中心实验室进行的 IHC 检测测定 FGFR2b≥10% 2+/3+ TC
6.东部肿瘤协作组(ECOG)体能状态评分为 0 至 1。
7.适当的器官功能如下:
Ÿ 中性粒细胞绝对计数≥1.5x10^9 /L
Ÿ 血小板计数≥100x10^9 /L
Ÿ 在研究治疗首次给药前 7 天内未输注红细胞(RBC)情况下,血红蛋白≥9 g/dl
Ÿ 天门冬氨酸氨基转移酶和 ALT<3×正常值上限(ULN)(如果累及肝脏,则<5×ULN)。总胆红素<1.5×ULN(如果累及肝脏,则<2×ULN;Gilbert病受试者除外)
Ÿ 使用 Cockcroft 和 Gault 公式[(140-年龄)×体重(kg)/(72×肌酐mg/dL)](如果是女性,×0.85)计算或测量的肌酐清除率(CrCl)≥30mL/分钟
Ÿ 国际标准化比值或凝血酶原时间(PT)<1.5×ULN,但接受抗凝剂治疗的受试者除外,受试者必须在入组前 6 周使用稳定剂量的抗凝治疗
8.可测量的疾病或不可测量,但根据 RECIST v1.1 可评估的疾病。
9.受试者无 mFOLFOX6 化疗禁忌症
排除标准
1.未治疗或有症状的中枢神经系统(CNS)转移软脑膜疾病
2.心脏功能受损或具有临床意义的心脏疾病
3.2 级或以上外周感觉神经病
4.研究治疗首次给药前 14 天及以内存在需要全身治疗的活动性感染或任何未控制的感染
5.已知 HER2 阳性状态(阳性定义为 IHC 检测为 3+或 IHC 为 2+和原位杂交阳性[ISH])
6.已知存在人类免疫缺陷病毒(HIV)感染且 CD4+T 细胞(CD4+)计数<350个细胞/μL,丙型肝炎感染或乙型肝炎感染
7.间质性肺疾病病史
8.既往或当前存在需要长期使用眼用皮质类固醇的全身性疾病或眼科疾病
9.任何持续性眼科异常或急性(4 周内)或持续进展的症状的证据
10.研究治疗期间不愿意避免使用隐形眼镜
11.研究治疗首次给药前 28 天内的重大手术操作
12.最近 2 年内其他恶性肿瘤史,以下除外:
Ÿ 已根治的非黑色素瘤皮肤恶性肿瘤
Ÿ 原位宫颈癌
Ÿ 1 期经根治性治疗的子宫癌
Ÿ 根治的原位导管或小叶乳腺癌,目前没有接受任何全身治疗
Ÿ 以根治为目的接受手术治疗且假定已治愈的局限性前列腺癌
13.有角膜缺损、角膜溃疡、角膜炎、圆锥形角膜、角膜移植史或其他已知的可能会增加发生角膜溃疡风险的角膜异常的证据或近期(6 个月内)病史。近期(6 个月内)接受过角膜手术或眼科激光治疗
注:以上为部分入排标准







发表评论